Tóm tắt ngắn: Tunneling nanotubes (TNTs) là các ống vi mô do màng tế bào tạo ra, nối trực tiếp bào tương của hai tế bào. Qua TNTs, tế bào có thể trao đổi protein, RNA, ion và thậm chí ty thể nguyên vẹn. Việc chuyển giao ty thể (mitochondrial transfer) qua TNTs đã được ghi nhận trong nhiều hệ mô — mở ra tiềm năng ứng dụng lớn trong y học tái sinh, điều trị tổn thương mô, và cả một số tác động bất lợi trong ung thư. Dưới đây là bài viết web chi tiết, có dẫn nguồn chính từ các nghiên cứu quan trọng và bài tổng quan gần đây.
Giới thiệu & tại sao TNTs quan trọng
Từ trước đến nay, giao tiếp tế bào thường được hiểu qua tín hiệu hoá học (cytokine, hormone), exosome, hoặc gap junction. Phát hiện về TNTs (một dạng ống màng mảnh, nâng lên khỏi bề mặt nền và kéo dài giữa hai tế bào) mở ra một dạng giao tiếp vật lý trực tiếp mới — cho phép truyền cả các bào quan như ty thể. Khái niệm này được gợi mở và lập luận từ những công trình nền tảng trong thập niên 2000. Bằng chứng thí nghiệm: ty thể có thể di chuyển giữa các tế bào
Bằng chứng thí nghiệm: ty thể có thể di chuyển giữa các tế bào
- Spees và cộng sự (2006) là một trong những bằng chứng sớm cho thấy mitochondria (hoặc mtDNA) có thể truyền giữa tế bào, khôi phục hô hấp hiếu khí ở tế bào nhận bị thiếu chức năng ty thể. Điều này thay đổi nhận thức về tính cố định của ty thể trong từng tế bào. PubMed
- Islam et al. (2012, Nature Medicine) trình bày bằng chứng in vivo: tế bào chất nền (bone-marrow-derived stromal cells / MSCs) có thể chuyển ty thể đến biểu mô phế nang bị tổn thương, góp phần bảo vệ chống chấn thương phổi cấp. Nghiên cứu này cho thấy trao đổi ty thể không chỉ xảy ra in vitro mà còn có ý nghĩa bệnh lý – sinh lý. PubMed
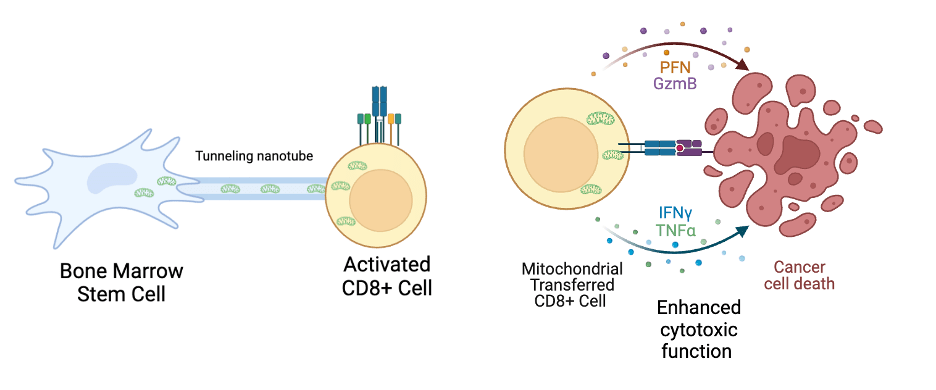
Những nghiên cứu sau đó (2014–2024) mở rộng quan sát này cho nhiều mô (tim, thần kinh, giác mạc…) và đặt nền tảng cho khái niệm “organelle medicine” — tận dụng sự chuyển giao bào quan để chữa bệnh. ScienceDirect+1
Cơ chế phân tử chính (tóm tắt)
Nhiều công trình đã làm sáng tỏ các thành phần và tín hiệu điều hòa quá trình hình thành TNTs và vận chuyển ty thể:
- Khung xương tế bào (actin, đôi khi microtubule) làm trục chính của TNTs; nhiều TNTs giàu F-actin. PMC
- Kênh gap junction / Connexin 43 (Cx43) đôi khi đóng vai trò trong trao đổi màng/vesicle, như báo cáo trong mô phổi. PubMed
- Miro1 (mitochondrial Rho-GTPase) là một trình điều khiển quan trọng giúp di chuyển ty thể dọc theo các sợi vi ống/actin và điều chỉnh xuất nhập ty thể giữa tế bào — nghiên cứu cho thấy điều chỉnh Miro1 làm thay đổi hiệu suất vận chuyển mitochondria từ MSCs sang tế bào đích. PubMed
- Các protein điều hòa hình thành TNTs (M-Sec, TNFAIP2, thymosin β4, v.v.) và các tín hiệu stress nội bào (ROS, Ca²⁺, mTOR, NF-κB) góp phần kích hoạt hoặc điều hướng quá trình này — các review gần đây tổng kết nhiều nhân tố này. PMC+1
-
Cơ chế vận chuyển ty thể — những điểm then chốt
- Kích hoạt: tổn thương hoặc stress (oxy hóa, thiếu oxy, viêm) ở tế bào đích làm tăng tín hiệu thu hút/đề nghị “giúp đỡ” (ví dụ ROS, cytokine), thúc đẩy tế bào cho/tế bào nhận hình thành TNTs. PMC+1
- Hình thành TNT: tế bào cho/điều phối tạo các nhánh màng dựa trên actin; cầu nối mở ra giữa hai tế bào. SpringerLink
- Vận chuyển ty thể: ty thể di chuyển dọc trục TNT, được hỗ trợ bởi các phân tử điều động như Miro1; ty thể có thể đi nguyên vẹn (kèm màng) hoặc trong các microvesicle/mitovesicle. PubMed+1
- Chấp nhận & hợp nhất: tế bào nhận tiếp nhận ty thể, tích hợp vào mạng lưới ty thể nội bào, cải thiện ATP, giảm apoptosis và phục hồi chức năng. PubMed+1
Ứng dụng lâm sàng tiềm năng (đã được nghiên cứu / đang phát triển)
Dưới đây là các hướng ứng dụng thực tế khả thi trong trung hạn — kèm ví dụ nghiên cứu minh họa:
- Phục hồi tổn thương phổi cấp (ALI/ARDS): chuyển ty thể từ MSCs giúp phục hồi biểu mô phế nang sau tổn thương — thử nghiệm tiền lâm sàng (Islam 2012). PubMed
- Phẫu thuật tim / bệnh lý tim mạch: mô hình cho thấy MSC hoặc tế bào hiến tặng có thể truyền ty thể giúp tế bào cơ tim bị thiếu oxy tăng cường sản xuất ATP và giảm hoại tử (nhiều nghiên cứu in vitro/in vivo). ScienceDirect+1
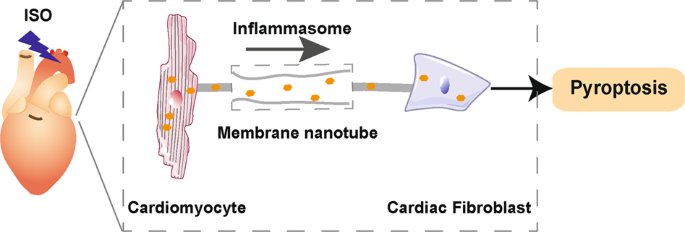
- Bệnh thần kinh thoái hóa (Parkinson, Alzheimer): ý tưởng là cung cấp ty thể khỏe cho tế bào thần kinh suy giảm nên giảm stress oxy hóa, tuy nhiên translational path còn dài và cần nhiều bằng chứng an toàn. ScienceDirect
- Hồi phục mô giác mạc, thận, cơ xương: báo cáo cho thấy lợi ích trong mô giác mạc, thận (một số nghiên cứu tiền lâm sàng & mô hình động vật). Nature+1
- “Organelle therapy” (thay thế/điều chỉnh ty thể): phát triển liệu pháp dựa trên cô lập + truyền ty thể hoặc tối ưu hóa khả năng trao đổi của tế bào hiến (engineering Miro1, tăng TNT formation) — đang là hướng nghiên cứu tích cực. ScienceDirect+1
Rủi ro, hạn chế & câu hỏi chưa lời giải
Rủi ro trong ung thư: tế bào ung thư có thể “mượn” ty thể khỏe từ tế bào xung quanh để gia tăng OXPHOS, tăng sức sống và kháng thuốc — do đó kích thích chuyển ty thể có thể là con dao hai lưỡi. PMC+1
- Kiểm soát chọn lọc: chưa rõ tế bào “chọn” ty thể nào được chuyển và cơ chế loại trừ ty thể nhiễm hại. PMC
- An toàn miễn dịch & di truyền: truyền ty thể có thể mang mtDNA khác haplotype — hệ quả lâu dài chưa được biết.
- Kỹ thuật sản xuất & phân phối: nếu mục tiêu là đưa ty thể tinh khiết (exogenous mitochondria) vào mô người, cần giải quyết vấn đề phân phối, tồn tại, và hợp nhất an toàn. SpringerLink
Hướng nghiên cứu ưu tiên (ngắn — trung hạn)
- Cơ chế chọn lọc & tín hiệu ‘give/receive’ — hiểu sao tế bào quyết định cho hay nhận. PMC
- Điều chỉnh phân tử (ví dụ Miro1, M-Sec) để tăng hiệu quả chuyển giao trong mô lành mạnh nhưng không thúc đẩy ung thư. PubMed+1
- Mô hình in vivo lớn & thử nghiệm an toàn trước khi chuyển sang thử nghiệm lâm sàng. PubMed
- Phát triển “mito-delivery platforms” (ty thể tinh khiết, vesicle chứa mito, hoặc tế bào kỹ thuật) để cung cấp theo hướng tiết kiệm rủi ro. ScienceDirect
Kết luận — tóm tắt ngắn
Trao đổi ty thể qua tunneling nanotubes là một khám phá khoa học có tầm ảnh hưởng lớn: nó mở ra phương thức cứu tế bào bị tổn thương bằng cách chuyển năng lượng nguyên vẹn, và đưa ra tiền đề cho “organelle medicine”. Tuy nhiên, lộ trình ứng dụng lâm sàng yêu cầu đánh giá rủi ro (đặc biệt trong ung thư), làm sáng tỏ cơ chế phân tử, và phát triển nền tảng kỹ thuật an toàn. ScienceDirect+4SpringerLink+4PubMed+4
Tài liệu tham khảo chính (chọn lọc)
- Rustom A., Saffrich R., Markovic I., et al. Nanotubular Highways for Intercellular Organelle Transport. Science. 2004. SpringerLink
- Spees J.L., Olson S.D., Whitney M.J., Prockop D.J. Mitochondrial transfer between cells can rescue aerobic respiration. PNAS. 2006. PubMed
- Islam M.N., Das S.R., Emin M.T., et al. Mitochondrial transfer from bone-marrow-derived stromal cells to pulmonary alveoli protects against acute lung injury. Nat Med. 2012. PubMed
- Ahmad T., Ikeda Y., Prasad K., et al. Miro1 regulates intercellular mitochondrial transport & enhances MSC repair function. (PMID 24431222). 2014. PubMed
- Baldwin J.G., et al. Intercellular nanotube-mediated mitochondrial transfer — organelle medicine perspective. Cell (review/analysis). 2024. ScienceDirect